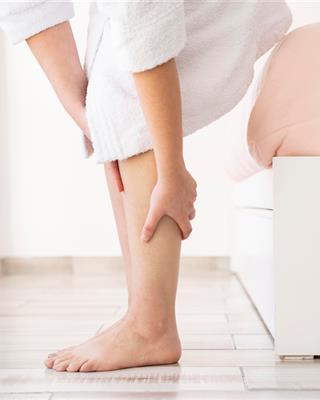
你應該要知道的食事
台灣2019年醫材產值預估約1,207億新臺幣,其中就有將近6成是輸出國外,實力不容小覷。未來醫材將從藥事法中獨立出來,政府用更透明與健全的法規,守護國民安全,推動產業進步。
口述=吳秀梅(衛生福利部食品藥物管理署署長)
採訪‧撰文=編輯部
全球各地陸續進入高齡社會,對醫療保健的需求逐年提升,醫療器材更是不可忽視的一環。台灣2019年醫材產值預估約1,207億新臺幣,其中就有將近6成是輸出國外,實力不容小覷。此外,我國血壓計、電動代步車與電動輪椅產品排行全球前三大,在國際間占有舉足輕重之角色。
貼合產業趨勢 修法與時俱進
為了讓台灣的醫材產業更上層樓,接軌國際,在食品藥物管理署(簡稱食藥署)積極推動下,有望在不久後迎來醫材的首部專法《醫療器材管理法》。未來醫材將從藥事法中獨立出來,政府用更透明與健全的法規,守護國民安全,推動產業進步。
「醫療器材推陳出新,很多過去沒有的醫療器材現在都出來了。」食藥署署長吳秀梅一語點出推動專法的急迫性。「科技日新月異,我們的法規也需要與時俱進,才能貼合產業需求與時代脈動。」
《醫材法》到底厲害在哪裡?署長吳秀梅表示,檢視全生命週期(Total product life cycle),從基礎研究到產品上市後監測,《醫材法》方方面面都不漏接,對業者與消費者而言都是利多。
醫材法上路 照顧全生命週期
署長吳秀梅表示,在設計階段,業者會根據病人需求設計醫材。隨著AI和ICT技術崛起,醫材不僅包含看得見的硬體,軟體也可視為醫材的一環。因此,未來設計業者也可以像製造業者一樣持有許可證,讓管理更全面。
1、特定品項的臨床試驗審查,速度將加快:
在臨床試驗階段,新法也打破過去齊頭式的審查方式,有更多彈性空間。過去,業者只要提供完整資料,有超過9成的查驗登記都在公告時間內完成審查,未來特定品項有機會變得更快。
2、部分低風險等級產品,電子登錄加速上市:
低風險或無顯著風險的第一等級產品,如一般的口罩和OK繃,業者不用再走查驗登記如此繁複的手續,可以用電子登錄加速上市時程,更早進入市場卡位。對民眾來說,也能早點享受更新的產品。
3、病患急需的新款醫材,經審查後可彈性發給許可證先上市:
又如病人若急需新款醫材,目前通過查驗登記,其可取得許可證效期為5年,新法上路後有彈性核給許可證效期之機制,在審查確認產品安全性,並搭配業者進行上市後臨床評估計畫(post-approval study)後,即可先讓產品上市,以嘉惠病患得及時使用最新醫療器材產品。
署長吳秀梅提醒,新法還包括要求醫材製造、輸入和維修業者聘用專業技術人員;推動優良運銷準則(GDP,Good Distribution Practice)強化管理醫材的運輸過程;因應自動販賣機和網購等新興販賣方式,規範相關販售方式及規則;明訂醫事機構和醫療器材商要建立產品流向管理機制,使醫材管理更上層樓。

接收第一手資訊 接軌國際
署長吳秀梅表示,從上述變革中不難發現,新法使醫材管理變得更加全面、彈性與透明,對業者和民眾而言都是福音。不僅如此,還能幫助台灣接軌國際,甚至是打國際盃。
「台灣的醫療器材在世界上是受肯定的,真的要給他們很多掌聲。」署長吳秀梅解釋,台灣的醫材頗具水準,派代表參加國際組織如國際醫療器材法規論壇(IMDRF)和亞洲醫療器材法規調和會(AHWP)等,不只是獲取第一手資訊,台灣的專業意見也經常被採納。《醫療器材管理法》參考他國先進法規修訂,使台灣能與國際接軌,業者佈局國際市場也更有機會。
「這個法上路後應該是全贏,可以照顧到很多人。」署長吳秀梅總結,新法上路後業者執行更於法有據,有更多機會佈局國際市場,民眾取得醫材也變得更方便,使得國人享受與國際同步的高水準醫材。
【食品藥物管理署廣告】
延伸閱讀
▶食藥署署長:為了幫臺灣保健食品走出國際,推動保健營養食品GMP勢在必行!
▶吃藥為了救命,吃錯就會害命!食藥署署長教你如何安全用藥
▶想到台灣的「高科技」只想到IT產業嗎?你所不知道的台灣醫藥研發服務實力其實更高端!